mRNA疫苗的體外穩定性
正如之前在背景介紹中提到的,目前已批準的 mRNA疫苗流通的主要障礙之一是它們必須以冷凍形式儲存。在 2–8 °C 的溫度下,輝瑞/BioNTech 和 Moderna 疫苗分別可穩定保存 5 天和 30 天,兩家公司都為終端使用提供了詳細的處理說明。有趣的是,據報道 CureVac 的候選疫苗在冰箱溫度和 -60 °C 下可穩定 3 個月。這些是目前發布了mRNA-LNP長期儲存條件的制造商,這種苛刻的溫度要求嚴重影響了這些疫苗的儲存、運輸和流通。然而,迄今為止,在公開資料中幾乎沒有關于優化mRNA 疫苗穩定性的信息。本節旨在概述影響 mRNA-LNP 疫苗成分穩定性的因素,并討論分析評價這種穩定性的方法。
mRNA穩定性
強烈影響所需儲存條件的主要因素是 mRNA 的穩定性。如上文2.1 節所述,mRNA 分子的結構經過專門設計可以用于增加體內靶抗原的翻譯。mRNA 的特殊性在于,即使是長 mRNA 鏈(通常長度在 1000 到 5000 個核苷酸之間)中的一個核苷酸發生變化(鏈斷裂或堿基氧化)便會導致翻譯終止。這使得 mRNA 疫苗與其他疫苗*不同,在其他疫苗中,抗原的微小變化不一定對其功效產生顯影響。因此,對于 mRNA 疫苗,監測整個分子的完整性是至關重要的。
mRNA 降解的方式有多種,可以分為化學和物理降解。化學降解包括 mRNA 分子中化學鍵的改變。物理不穩定性包括變性(二級和三級結構的喪失),與變性對蛋白質生物制劑活性的影響不同,物理不穩定性對mRNA的影響可能不太明顯。然而,變性還包括聚集和沉淀等變化,這些變化會影響mRNA的翻譯表達。在一篇關于核酸穩定性的綜述中,Pogocki 和 Sch?neich 指出化學降解在siRNA降解中的影響比物理不穩定性更大,對于鏈長更長的 mRNA來說可能更是如此。
mRNA在體外的化學降解主要包括水解和氧化,水解主要是發生在mRNA 分子骨架的磷酸二酯鍵(圖5 )。核糖上的2' OH 基團起著至關重要的作用,因為導致 mRNA 鏈斷裂的酯交換反應起始于磷酸酯鍵上的 2'OH 基團的親核進攻導致 P-O5' 酯鍵斷裂(圖5)。這個過程需要水,可以被核酸酶催化,也可以被 mRNA 分子本身和其他外源因素如酸和堿催化。在有關 mRNA 水解的兩篇文獻中,作者指出 mRNA 的堿基序列和二級結構會影響水解速率。具體而言,堿基堆積可能會降低磷酸二酯鍵的裂解速率,可以小化 mRNA 分子的“平均未配對概率"。可以使用專門設計的算法來選擇可以形成大雙鏈區域的單鏈 mRNA 的核苷酸序列。據稱,采用這種方法優化后,體外穩定性得到了改善。
CureVac、輝瑞/BioNTech 和 Moderna 疫苗之間的區別在于后兩者具有 1-甲基-假尿苷的單核苷摻入。之前的一項研究表明,這種修飾提高了 RNA 二級結構的穩定性。CureVac 采用提高GC比例策略,具有類似的效果。
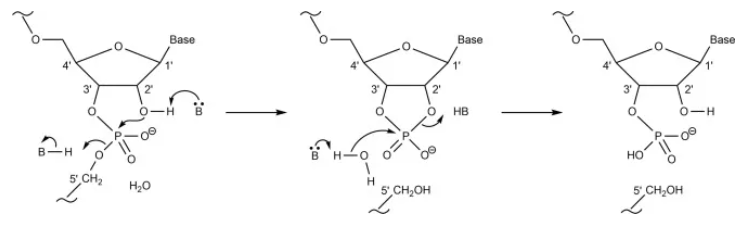
圖5 通過 2',3'-環狀磷酸酯,堿基催化RNA分子內的磷酸二酯鍵水解、B表示Br?nsted堿。
相反,氧化會影響堿基,并在較小程度上影響mRNA 核糖單位的糖基團。氧化可導致堿基裂解、鏈斷裂和 mRNA 二級結構的改變。然而,如前所述,水解似乎被認為是驅動 mRNA 降解的關鍵因素。